
接上(第一篇)~
4、电化学表征
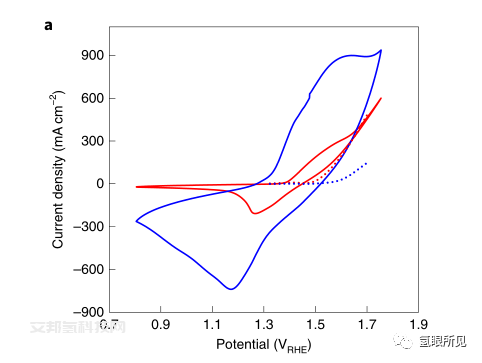
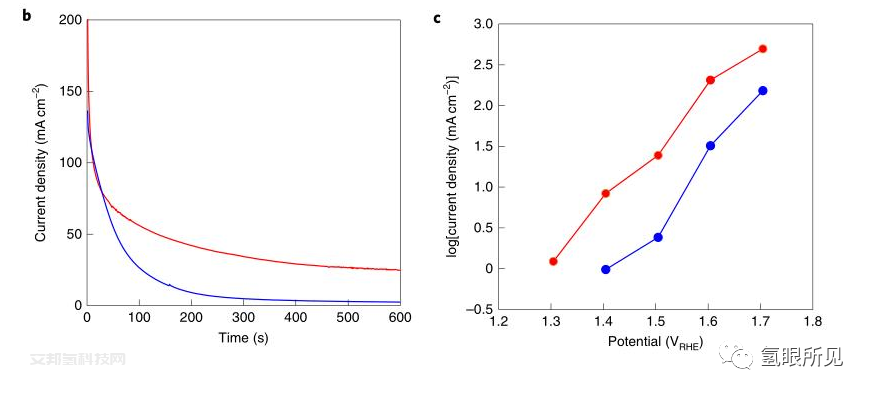
Ni0.9Co0.1(OH)2和NiFe LDH阳极的电化学性能说明:
图a,在50 mV/ s的扫描速率下测量的循环伏安图。
图b,计时安培电流痕迹为1.48 VRHE。
图c, Tafel图是稳态水氧化电流与电位的函数,从10分钟安培电流图,如b中所示。
虚线a表示从c中提取的稳态水氧化电流。对于所有图,Ni0.9Co0.1(OH)2阳极用蓝色表示,NiFe LDH阳极用红色表示。所有试验均在5 mol/L KOH环境温度下进行。
备注:塔菲尔(Tafel)图是表示电极电位与极化电流或极化电流密度之间的关系。
为了确定Ni0.9Co0.1(OH)2阳极充电反应的法拉第效率,我们首先比较了电容电荷与计时安培充电过程中流动的总电荷。在1.48 VRHE的电位下对完全放电的阳极充电时,法拉第效率大于99.7%,持续时间超过2000秒,在此期间阳极充电超过50 C /cm2。为了验证不产生氧气,在1.48 VRHE恒电位下对完全放电的阳极充电时,监测电解液中的溶解氧浓度。在55 C/ cm2的电荷范围内,没有观察到溶解氧浓度上升。
在尽可能类似于E-TAC工艺的产氢步骤的条件下(即在恒电流下给阳极充电),也对溶溶氧浓度进行监测。此外,在1.48 VRHE再生Ni0.9Co0.1(OH)2阳极时安培充电下,还测量了溶解氧浓度。在这两种情况下,在3 C/ cm2以上的溶解氧浓度没有上升,确认在这些条件下阳极充电时没有产生氧气。最后,气相色谱测量显示,在固定电流密度为50 mA/cm2(即充电5 C/ cm2)的情况下,阳极密封电池的顶空氢气浓度上升,而氧气浓度没有上升。这些结果证实了在E-TAC制氢过程中,阳极充电时没有发生析氧等寄生副反应。
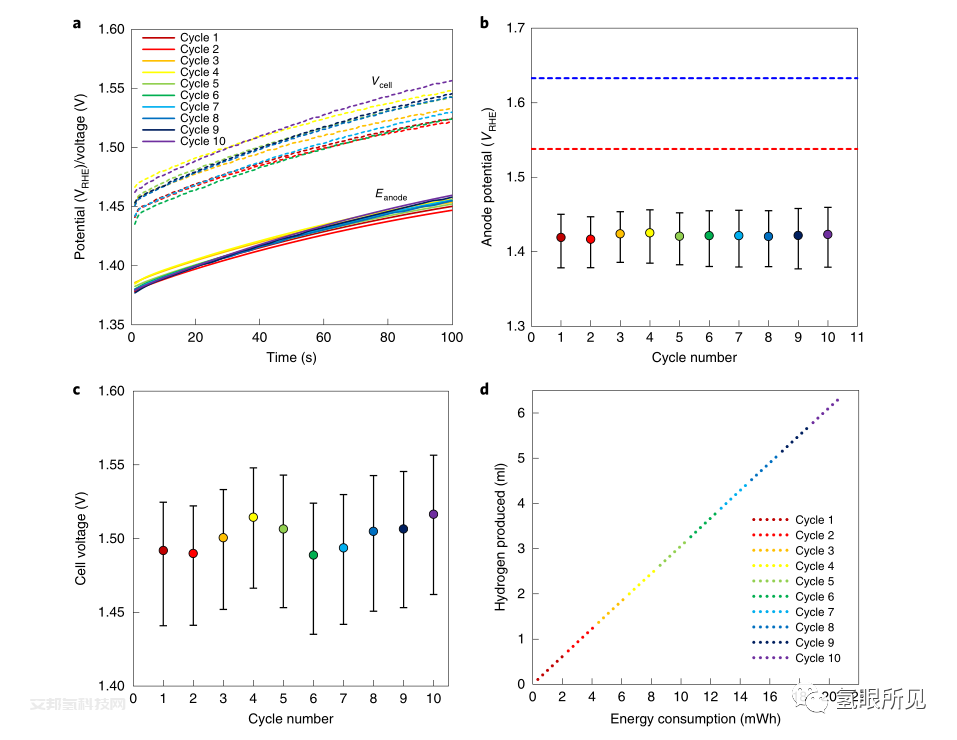
在E-TAC的概念验证实验中,氢气在镀镍不锈钢阴极上产生,而Ni0.9Co0.1(OH)2阳极在5 M KOH水溶液(pH 15)中氧化为Ni0.9Co0.1(OH)2。采用了Ni0.9Co0.1(OH)2阳极,再生容量为5 C/ cm2。产氢步骤在环境温度下进行(不加热或冷却),电流密度为50 mA/ cm−2,时间为100 s。我们将施加的电池电压限制在不超过120 mV的热中性电压(1.48 V)。这有助于最大限度地减少热损失,并防止氧的产生和阳极过充,这可能使NiO(OH)从β相转变为γ-p相。根据溶解氧测量,对于该电荷量,阳极充电反应的法拉第效率为99.2%±0.1%。在制氢(充电)步骤期间记录了电池电压Vcell和阳极电位Eanode,如下图a所示:
每100 s产氢步骤结束后,将带电阳极从冷电池中取出,置于热(T = 95°C)电解液(5 M KOH)中100 s,以加速自发释氧和初始状态的再生。在阳极再生步骤中观察到明显的气泡(O2)形成,而在氢气生成步骤中,气泡(H2)只在阴极上形成。
在每个充电步骤中,电池电压和阳极电位以一致的方式增加,从一个循环到另一个循环显示出很少的变化,没有稳定的漂移(图3a)。这种电化学行为表明,该过程是循环的,没有降解;在每个循环结束时,阳极的SOC返回到初始状态,没有可测量的变化。为了证实这一点,在E-TAC循环之前、期间和之后,通过原位显微结构(SEM)和结晶度(x射线粉末衍射)分析验证了阳极的循环性。
在制氢步骤中,阳极电位从1.37-1.45 VRHE(下图a)变化,远低于Ni0.9Co0.1(OH)2和NiFe LDH阳极的OER电位(分别由下图b中的蓝色和红色虚线表示)。在这些电位下,氧的析出可以忽略不计。电池总电压从1.44-1.56 V变化(下图a),在所有10个周期中平均为1.5 V(下图c)。E-TAC过程的电压效率36,Vth/Vcell,其中Vth为水裂解反应的热中性电压(标准条件下为1.48 V),在所有10个循环中平均为98.7%。由电流×时间乘积(即电荷)可以计算出,在下图所示的十次循环中产生了6.4 ml氢气(1 atm, 25°C),根据循环中测量的电流和电池电压消耗20.8 mWh,如下图所示。因此,E-TAC工艺实现了较低的电能消耗,仅为3.24 kWh /m3,或39.9 kWh/ kg氢气。

7.碳酸盐缓冲电解质溶液中的E-TAC水分解
因此,还通过在pH值为10.6的碳酸盐-碳酸氢盐(K2CO3:KHCO3的3:2比例)缓冲电解质中操作来证明该方法的多功能性。在该试验中,在25 mA /cm2的标称电流密度下,阳极电位从1.43–1.50VRHE变化。这表明E-TAC水裂解工艺不仅限于碱性溶液,在电化学工业中具有更广泛的应用潜力。
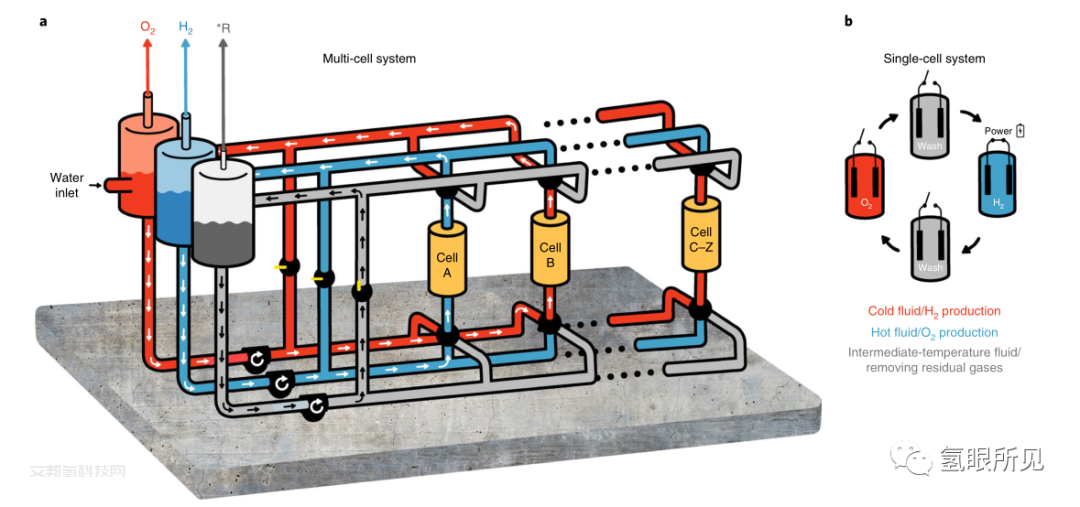
多单元E-TAC过程示意图:
a,过程中一般的电解液流动,图中为冷电解质在a槽内循环,产生左侧中间(蓝色)槽相分离的H2气体,而热电解质在B槽内循环,产生左侧红色槽相分离的O2气体。左边灰色槽中的中温洗涤液大部分时间通过旁路循环。该液体用于将冷电解质溶液和热电解质溶液“推”到生成H2或生成O2步骤结束时各自的槽中。
b,单电池循环,显示每个电池的再生操作,H2在环境温度下的电偏置下产生,O2在不施加电偏置的更高温度下产生(开路)。
* R,表示残余气体。
未完待续,敬请期待~
原文始发于微信公众号(氢眼所见):关于H2Pro这家电解水企业以及E-TAC技术路线的介绍(第二篇)
 艾邦氢能产业链通讯录,目前有2200人加入,如亿华通、清极能源、氢蓝时代、雄韬、氢牛、氢璞、爱德曼、氢晨、喜马拉雅、明天氢能、康明斯、新源动力、巴拉德、现代汽车、神力科技、中船712等等,可以按照标签筛选,请点击下方关键词试试
资料下载:
艾邦氢能产业链通讯录,目前有2200人加入,如亿华通、清极能源、氢蓝时代、雄韬、氢牛、氢璞、爱德曼、氢晨、喜马拉雅、明天氢能、康明斯、新源动力、巴拉德、现代汽车、神力科技、中船712等等,可以按照标签筛选,请点击下方关键词试试
资料下载:


