
理想热化学
理想热化学
电解水反应是一种涉及热力学变化的过程。在这个过程中,质量和能量是守恒的。考虑一下示例中图1的试验装置,可以在恒定的工作温度和压力下分析反应的热能。将电解设备放置在等温恒温器内,并使化学物质在电解设备中保持恒定压力。
假定反应在接近平衡条件下进行,即没有内部损耗,此时在温度TT 和压力 pp 条件下,热能的转换可由吉布斯-亥姆霍兹方程表示:
∆H(T,P)=∆G(T,P)+T∆S(T,P) (1)
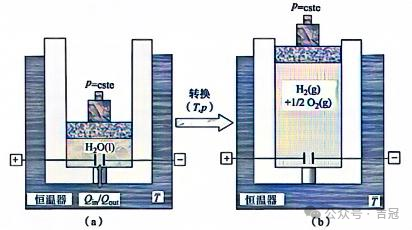
图1 恒温恒压条件下电解水转换示意(图中:+表示正极,-表示负极)
(a)初始状态;(b)最终状态
焓变ΔH代表分解1摩尔水分子所需的总能量。由于分子数目的增加以及液态转变为气态,熵变 ΔS为正值。在恒定温度下,由于熵增加所需要的热能可以用 TΔS表示。因此,上述表达式(1)描述的是分解1摩尔水所需的电能 ΔG。
此外,式(1)还显示了在恒定温度 T 和压力 p 下,反应的热力学特性是 T 和 p 的函数。从工程的角度来看,感兴趣的温度范围介于环境温度(在接近环境温度下电解液态水)和900℃(固体氧化物水电解,S0WE)之间。在化学工业中,实际可应用的压力上限可达到800 bar(例如为了提高燃料电池车的机动性)。然而,在如此高压力下进行电解水会产生额外的成本,因此高压电解槽通常的工作压力限制在50~100 bar,并与机械压缩机相连。
1.工作温度的影响
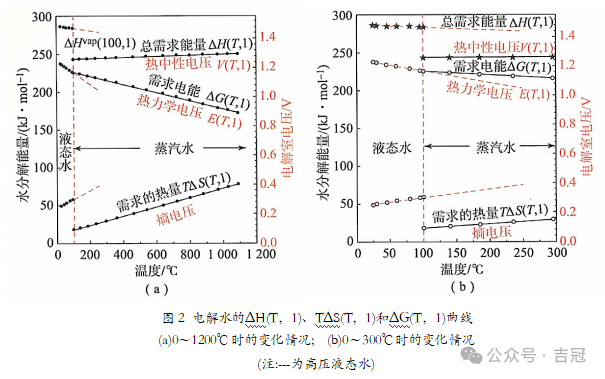
在整个关注的(T,p)范围内,水分解反应是一个吸能(非自发)过程。图2总结了1bar时的普遍情况。
在该范围内,总能量需求△H(T,p)几乎是恒定的,在(100℃,1bar)的不连续性是由于水汽化造成的;熵变也几乎是恒定的,(在100℃,1bar)时的不连续性也是由于水汽化造成的,熵变所需的热量是温度的线性函数。由于这种趋势,吉布斯自由能变△G(T,p)随T减小(随p增大,如下所述)。为了比较,图2总结了100℃以上高压液态水电解的普遍情况(虚线)。在这种情况下,分解水所需的能量更大,因为水仍然是液态。当然有一个压力极限,超过这个极限是不可能的,因为压力会随着温度的升高而迅速增加。电解水温度可以提高到150℃,这是在更高的动力学、最小的腐蚀性和高压带来的额外成本最小之间的一个很好的折中。
2.工作压力的影响
假设电解水生成的是干燥和理想的气体(实际情况需要校正),考虑基础热力学,工作压力对水分解反应热化学的影响如下。
在(T,p)条件下,假设理想气体为n mol,水分解系统的吉布斯自由能的微分形式为
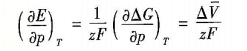 (2)
(2)
根据热力学第一定律和热力学第二定律
dG=Vdp(FP)+SdT(SP) (3)
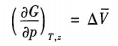 (4)
(4)
式中:Δ`V为与压力变化相关的摩尔体积变化;z为总反应中交换的电子数。
设E为电解室电压,则
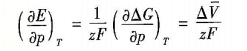 (5)
(5)
考虑到压力对液态水体积的影响很小,A元仅考虑气态物种。假设这些气体
是理想的,则
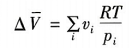 (6)
(6)
式中:R为理想气体常数;p;和v;分别为物种i的分压和化学计量系数,则
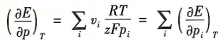 (7)
(7)
在恒定工作温度下,从参考分压po积分,得
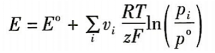 (8)
(8)
应用于电解水,有
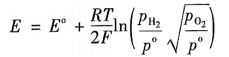 (9)
(9)
设po为大气压力,p为电解水系统总压力。忽略H₂和O₂中水蒸气的饱和压力,并假设阳极po2=p,阴极PH₂=p(当电解室在阳极室和阴极室中均以恒压平衡工作时),得出以下关系:
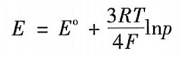 (10)
(10)
当压力从p到p2的变化时,电解室的电压变化为
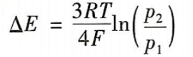 (11)
(11)
在这种假设下,应用理想气体的一般热状态方程,推导了电解水关注的(7,p)范围内的压力修正的热力学函数。图3所示为电解水关注的(T,P)范围的热力学电压E(T,p)的关系简化图。
这些数据有助于确定电解水最关注的(7,p)范围吗?答案是肯定的,但也不完全。其他因素(如电解室材料的可用性、成本和稳定性、反应动力学)也需要考虑。通过粗浅分析可以得出结论:在高温(600~900℃)下分解水比在近环境温度(NAT)的条件下分解水更为有利,因为大约1/3的总能量需求可以由热量提供。当使用热机发电时,电能是热能的4~5倍。当使用可再生能源(太阳能电池板或风力涡轮机)时,情况并非如此,且在600~900℃温度下,火用含量(ExergyContent,EC)远高于NAT的火用含量。在比较NAT和高温电解水技术时,需要考虑上述因素。
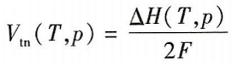
图3 电解室热力学电压E(T,P)关系简化图
近环境温度(NAT)的条件下分解水更为有利,因为大约1/3的总能量需求可以由热量提供。当使用热机发电时,电能是热能的4~5倍。当使用可再生能源(太阳能电池板或风力涡轮机)时,情况并非如此,且在600~900℃温度下,火用含量(Exergy Content,EC)远高于NAT的火用含量。在比较NAT和高温电解水技术时,需要考虑上述因素。
非理想热化学
对理想热化学进行修正:①电解水过程中产生水蒸气饱和气体;②气体压力大于10bar时,不能作为理想压力处理。
1、水蒸气的影响
电解室或电解槽制取的气体被水蒸气饱和。在气体排出条件(T,p)下,热力学电压的表达式可以通过这些气体的分压修正,分压简单处理为电解室总压力和水饱和压力之间的差值:
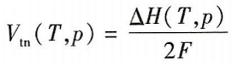 (12)
(12)
式中:pA为阳极室总压力(Pa);pC为阴极室总压力(Pa);psatH2O是(T,p)条件下水的饱和压力(Pa)。上标A、C和sat分别代表阳极、阴极和饱和。
因此,通过水蒸气分压降低反应物(H2和O2)的分压,可以降低电解过程中的电能需求,但还需要能量对气体进行干燥,以便于下游应用(如储气)。
2、压力引起的非理想效应
由压力增加产生的非理想效应可以通过使用对真实气体有效的热状态方程来评估。Hanke-Rauschenbach等在Handbook of Hydrogen Energy中发表了理想的、干燥的和湿润的氢气和氧气的热力学电压与工作压力p(bar)的函数关系图。与参考情况(理想和潮湿)的偏差随着工作压力p的增加而增加。在压力100bar和温度60℃时,忽略非理想性,将低估1.3%的能源需求,高估9.7%的热量需求。
电化学热力学
电解水反应是一个吸能过程。这意味着在恒温恒压条件下,标准吉布斯自由能变为正。如上所述,在更大范围(T,p)工作条件下,这种情况普遍存在。然而,电解反应可以通过提供等量的电能来进行。根据热力学第一定律(能量守恒定律),在(7,p)条件下分解1mol水所需的电量等于在相同(T,p)条件下电解水反应的吉布斯自由能变:
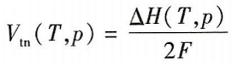 (13)
(13)
式中:△G(T,p)为(T,p)条件下,电解水反应的吉布斯自由能变;F是法拉第常数,96485.33C/mol;E为电解室的热力学电压(V)(在可逆、非耗散条件下,电解水转换的电解室电压)。
因此,E(T,p)是需要作用在电解室上的最小电压,此时可以观察小电流在电解室流动。仔细观察这一情况可以发现,在恒定(T,p)条件下,需要提供给电解室分离1mol水的能量实际上是电能△G和热能(T△S)的总和。因此,很方便引入热中性电压Vtn(T,p),即
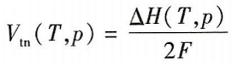 (14)
(14)
式中:△H(T,p)为(T,p)条件下,电解水反应的焓变;F为法拉第常数;Va为电解室水分解的热中性电压(V),下标tn表示热中性(thermoneutral)。
在实际工作条件(j≠0)下,Ucell(T,p)为电解室上作用的电压。根据热力学电压、热中性电压和电解室电压之间不同的关系,电解室有以下3种工作情况。
(1)Ucell(T,p)<E(T,p),电解室内没有电流,不会发生电解水。
(2)E(T,p)<Ucell(T,p)<Vtn(T,p),电解室内有净电流,发生电解水。然而,电解室内耗散不足以提供所需的热能。在这个电压范围内,电解室在吸热模式下工作。
(3)Ucell(T,p)>Vtn(T,p),大量电流流经电解室,电解水反应速度更快。由于内耗散产生的热量比(T,p)条件下所需焓变的能量更多,过多的热量将散发到环境中。在这个电压范围内,电解室工作在放热模式。
因此,热中性电压是由于内耗散而由直流电源提供熵增加所需热量的电压。图2显示了E(T,1bar)和V(T,1bar)在适用温度范围内的曲线。
吉冠氢能
苏州吉冠科技有限公司,成立于2021年,专注于氢能制取和应用的成套解决方案。公司主营业务包括ALK低压高电密电解槽(方形),这种电解槽提供预组装的橇装模块化电解装置,有助于简化新制氢厂的建设并保持较低成本。目前,橇装模块化的电解装置可通过累加实现吉瓦级的产能需求,适用于大规模制氢。


谢谢大家关注!
原文始发于微信公众号(吉冠):电解水温度与压力对能量效率的影响


